Revisão — Funções da Química Inorgânica
Ácidos
É toda e qualquer substância que em solução aquosa libera como único cátion H+
Propriedades
-Sabor azedo;
-Condutibilidade elétrica;
-Presença de H à esquerda da molécula;
-Reagem com metais liberando hidrogênio;
-Reagem com base formando sal e água.
Classificação
Quanto ao número de hidrogênios ionizáveis
-Monoácidos;
-Diácidos;
-Triácidos;
-Tetrácidos.
Quanto a presença de oxigênio
-Hidrácidos;
-Oxiácidos.
Quanto ao grau de ionização - Hidrácidos
-Fracos: a <= 5%;
-Moderados: 5%< a < 50%;
-Fortes: a >= 50%
Quanto ao grau de ionização - Oxiácidos
-X=Nº de átomos de oxigênio - Nº de hidrogênios ionizáveis
Nomenclatura dos ácidos
Ácido + nome do elemento + ídrico
-HF = Ácido Flurídrico;
-HC = Ácido Clorídrico;
-HB = Ácido Bromídrico.
Orto - Meta - Piro por grau de hidratação
-Ácido Orto - Maior Grau de Hidratação (ex: H3PO4 - Ácido Ortofósrico (-1 H2O));
-ácido Meta - Retirada de uma molécula de água do ácido orto (e: HPO3 - Ácido Metasfórico)
-Ácido Piro - De duas moléculas de ácido orto retira-se uma molécula de água (ex: H3PO4 x 2 = H6P2O8 - 1H20 = H4P2O7 Ácido Pirosfórico).
Oxiácidos e demais ácidos
Ácido + elemento formador + ato ou ico
-Reação de ionização - tabela dos ânions
1 - Elementos que possuem uma única valência
2 - Elementos que possuem duas valências
3 - Elementos que possuem várias valências
Tabelas
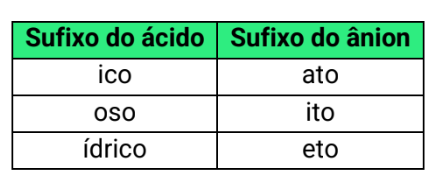
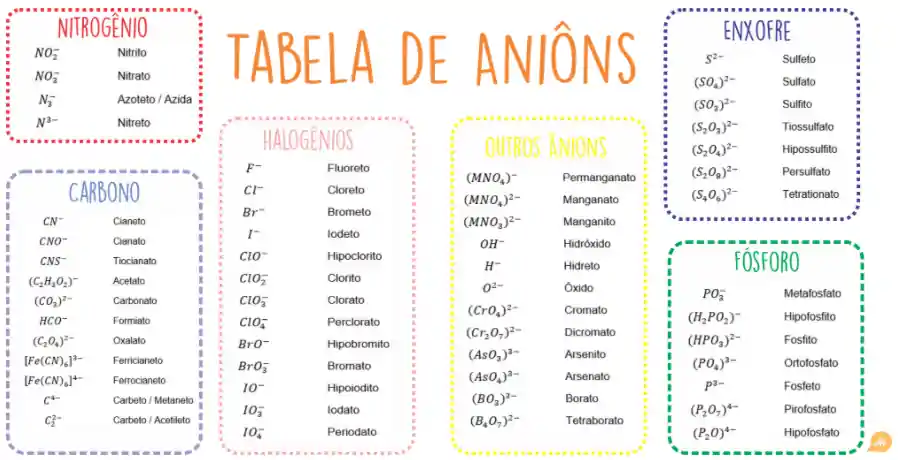
.
.
Clique para revelar a resposta
Carregando...
[ clique para ver a resposta ]
1 / 35